กรด vs เบส ออกสอบบ่อย!
สวัสดีน้อง ๆ ชาว Dek-D ทุกคนค่ะ วันนี้เรามาพบกันในคอลัมน์ “รู้ไว้เผื่อออกสอบ” โดยวันนี้พี่ได้นำวิชาเคมีมาฝากน้อง ๆ ทุกคนกันค่ะ และในวิชาเคมีวันนี้เรามาพบกันในเรื่อง กรด-เบส โดยเรื่องของ กรด-เบส เป็นเรื่องที่น้อง ๆ สามารถเจอได้ในผลิตภัณฑ์ต่าง ๆ ที่เราใช้ในชีวิตประวัน และยังออกสอบบ่อยอีกด้วย!!! ถ้าน้อง ๆ พร้อมแล้ว เราไปทำความรู้จักกับเรื่อง กรด-เบส กันเลยค่ะ

กรด-เบสมีกี่ประเภท?
กรด
1. กรดอินทรีย์ : กรดที่เป็นสารประกอบอินทรีย์ จะมีโครงสร้างที่ประกอบด้วยหมู่ฟังก์ชัน ดังนี้

ตัวอย่าง กรดแอซีติกหรือกรดน้ำส้ม มักจะใช้ในน้ำส้มสายชู
กรดซิตริก กรดที่พบได้ในผลไม้ที่มีรสเปรี้ยว
2. กรดอนินทรีย์ : สามารถเรียกอีกอย่างว่ากรดแร่ โดยจะแบ่งออกเป็นประเภทย่อยได้หลัก ๆ 2 ประเภท คือ กรดไฮโดร และกรดอ็อกซี
ตัวอย่าง กรดเกลือ กรดดินประสิว กรดหินปูน ฯลฯ
เบส
1. เบสอินทรีย์ : เบสที่เป็นสารประกอบอินทรีย์ จะมีโครงสร้างที่ประกอบด้วยหมู่ฟังก์ชัน ดังนี้
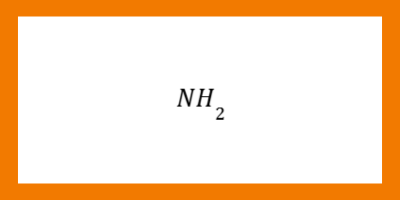
ตัวอย่าง เบสที่ได้จากธรรมชาติ หรือสารประกอบเอมีน เช่น แอมโมเนีย นิโคติน
2. เบสอนินทรีย์ : มักเป็นสารประกอบไอออนิกของโลหะหมู่ 1 และหมู่ 2
ตัวอย่าง ได้มาจากสิ่งไม่มีชีวิต เช่น โซดาไฟ
คุณสมบัติของสารละลายกรด-เบส มีอะไรบ้าง?

กรด | เบส |
กรดมีรสชาติเปรี้ยว | เบสมีรสชาติเฝื่อน หรือฝาด |
กรดสามารถนำไฟฟ้าได้ดี เนื่องจากกรดสามารถแตกตัวเป็นไฮโดรเจนไอออน | เมื่อเบสทำปฏิกิริยากับน้ำมันพืชจะได้สารละลายที่มีฟองคล้ายกับสบู่ |
กรดมีคุณสมบัติในการกัดกร่อนโลหะ หินปูน เนื้อเยื่อของร่างกาย | เมื่อทำปฏิกิริยากับแอมโมเนียมไนเตรต(มักใช้ในเกษตรกรรม จะพบในปุ๋ย) จะได้แก๊สที่มีกลิ่นฉุนของแอมโมเนีย |
กรดทำปฏิกิริยากับหินปูนทำให้หินปูนกร่อน และจะได้คาร์บอนไดออกไซด์ ซึ่งสามารถทำให้น้ำปูนใสขุ่นได้ | สามารถกัดกร่อนโลหะ อลูมิเนียม สังกะสี |
กรดทำปฏิกิริยากับเบสได้เกลือ และน้ำ | เบสทำปฏิกิริยากับกรด ได้เกลือและน้ำ เช่น โซดาไฟ ทำปฏิกิริยากับกรดเกลือได้เกลือแกงที่ใช้ปรุงอาหาร หรือ โซดาไฟ + กรดไขมัน = สบู่ |
กรดทำปฏิกิริยากับโลหะบางชนิดได้ ไฮโดรเจนซึ่งสามารถติดไฟได้ | |
เปลี่ยนกระดาษลิตมัสจากน้ำเงินเป็นแดง | เปลี่ยนกระดาษลิตมัสจากแดงเป็นน้ำเงิน |
ทฤษฎีกรด-เบส

- ทฤษฎีกรด-เบสของอาร์เรเนียส (Arrhenius)
- ทฤษฎีกรด-เบสของเบรินสเตด-ลาวรี (Bronsted-Lowry)
- ทฤษฎีกรด-เบสของลิวอิส (Lewis)
โดย 3 ทฤษฎีกรด-เบสจะเป็นอย่างไรบ้าง หรือต่างกันอย่างไร เราไปดูกันเลยค่ะ
1. ทฤษฎีกรด-เบสของอาร์เรเนียส (Arrhenius)
- กรดเป็นสารประกอบที่มี H และเมื่อละลายน้ำจะแตกตัวให้
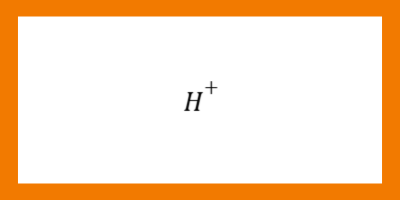
- เบสเป็นสารประกอบที่มี OH และเมื่อละลายน้ำจะแตกตัวให้
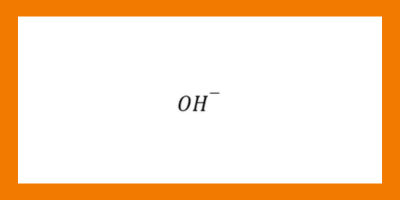
ข้อจำกัด ทฤษฎีกรด-เบสของอาร์เรเนียส

ตัวอย่าง ทฤษฎีกรด-เบสของอาร์เรเนียส

2. ทฤษฎีกรด-เบสของเบรินสเตด-ลาวรี (Bronsted-Lowry)
- กรด สารที่สามารถให้โปรตอนแก่สารอื่น
- เบส สารที่สามารถรับโปรตอนจากสารอื่น
ตัวอย่าง ทฤษฎีกรด-เบสของเบรินสเตด-ลาวรี

3. ทฤษฎีกรด-เบสของลิวอิส (Lewis)
- กรด คือ สารที่สามารถรับอิเล็กตรอนคู่โดดเดี่ยวจากสารอื่น
- เบส คือ สารที่สามารถให้อิเล็กตรอนคู่โดดเดี่ยวแก่กรด
ตัวอย่าง ทฤษฎีกรด-เบสของลิวอิส

กรดแก่ และกรดอ่อน คืออะไร?
กรดแก่ : กรดที่มีค่า pH ต่ำ มีการแตกตัว100% และเกิดปฏิกิริยาไปข้างหน้าอย่างเดียว ได้แก่ กรดไฮโดร (กรดอนินทรีย์ที่ไม่มีออกซิเจนเป็นตัวประกอบ) กรดอ็อกซี (กรดอนินทรีย์ที่มีออกซิเจนเป็นตัวประกอบ) เช่น กรดซันฟิวริก กรดไฮโดรคลอริก ฯลฯ
กรดอ่อน : กรดที่มีค่า pH สูง และสามารถแตกตัวได้บางส่วน และเกิดปฏิกิริยาย้อนกลับ เช่น กรดแอซีติก กรดไนตรัส ฯลฯ
การแบ่งชนิดของกรด-เบส
กรด แบ่งชนิดตามการแตกตัว

เบส แบ่งตาม จำนวน OH

การไทเทรตกรด-เบส
การไทเทรตกรด-เบสคือการนำสารตัวอย่างที่ต้องการมาไทเทรตกับกรด หรือเบสที่ทราบความเข้มข้นที่แน่นอน แล้วสังเกตสีของอินดิเคเตอร์ที่เปลี่ยนไป โดยการที่เราเลือกใช้อินดิเคเตอร์ที่เหมาะสม จะสามารถบอกจุดยุติที่ใกล้เคียงกับจุดสมมูลได้
อินดิเคเตอร์ คือ สารที่ใช้ในการทดสอบความเป็นกรด-เบส ของสารละลาย
จุดยุติ คือ จุดที่อินดิเคเตอร์เปลี่ยนสีขณะไทเทรต
จุดสมมูล คือ จุดที่กรดและเบสทำปฏิกิริยากันพอดี
การไทเทรต จะแบ่งได้ 4 แบบ โดยการไทเทรตแต่ละแบบจะให้ผลลัพธ์ที่ต่างกันออกไป ดังนี้
- การไทเทรต กรดแก่ - เบสแก่
- การไทเทรต กรดอ่อน - เบสแก่
- การไทเทรต เบสอ่อน - กรดแก่
- การไทเทรต กรดอ่อน - เบสอ่อน
สารละลายบัฟเฟอร์
สารละลายบัฟเฟอร์มีสมบัติในการควบคุม pH ให้มีการเปลี่ยนแปลงเพียงเล็กน้อยเท่านั้น เมื่อเติมกรด เบส น้ำลงไป โดยบัฟเฟอร์มักจะถูกใช้ในชีวิตประจำวัน เช่น สารกันบูดที่ใส่ในอาหารสำเร็จรูป เป็นต้น
กรด-เบส ที่พบได้ในชีวิตประจำวัน?
- กรด กรดกำมะถัน, น้ำส้มสายชู, ผลไม้รสเปรี้ยว, น้ำยาล้างห้องน้ำ ฯลฯ
- เบส ยาลดกรดในกระเพาะอาหาร, ยาถ่าย, ปุ๋ย, น้ำยาปรับผ้านุ่ม, ผงซักฟอก, สบู่ ฯลฯ
- สมบัติเป็นกลาง น้ำหอม, สเปรย์ฉีดผม ฯลฯ
สำหรับน้องๆ ที่ยังไม่แม่นเนื้อหา ฟิตความพร้อมก่อนสอบด้วย คอร์สพิชิต TCAS เคมี A-Level สรุปเนื้อหาเคมี ม.ปลาย 3 ปี ครบถ้วน ตรงตามหลักสูตรล่าสุด สสวท. ตัวอย่างโจทย์จัดเต็มกว่า 340 ข้อ เทคนิคการทำโจทย์แบบเข้าใจจริง เน้นย้ำจุดที่พลาดได้บ่อยๆ คอร์สนี้สอนโดย อ.เต้ อาจารย์ประจำภาควิชาเคมี จุฬาฯ
มาทดสอบความรู้กัน!
ทำความเข้าใจเรื่องกรด-เบสกันไปแล้ว ถึงเวลามาทดสอบความรู้กันแล้วค่ะ ถ้าพร้อมแล้วเริ่มทำได้เลย!
ข้อ 1
ในชั่วโมงวิทยาศาสตร์ นักเรียนได้ทำการทดลองโดยใช้กระดาษลิตมัสทดสอบความเป็นกรด-เบส และใช้ pH Meter วัดค่า pH ของเหลว 5 ชนิด ได้แก่ น้ำส้มสายชู, น้ำยาล้างจาน, น้ำดื่ม, น้ำอัดลม และสารละลายโซดาไฟ ดังนี้
| ชนิดสารละลาย | ผลการทดสอบกระดาษลิตมัส | ค่า pH |
| น้ำส้มสายชู | ไม่เปลี่ยนสีกระดาษลิตมัสสีแดง | A |
| น้ำยาล้างจาน | เปลี่ยนสีกระดาษลิตมัสสีแดงเป็นน้ำเงิน | B |
| น้ำเปล่า | ไม่เปลี่ยนสีกระดาษลิตมัส | C |
| น้ำอัดลม | เปลี่ยนสีกระดาษลิตมัสสีน้ำเงินเป็นแดง | D |
| สารละลายโซดาไฟ | ไม่เปลี่ยนสีกระดาษลิตมัสสีน้ำเงิน | E |
ข้อใดเรียงลำดับค่า pH จากน้อยไปมากได้ถูกต้อง
1. E < A < D < C < B
2. A < D < C < B < E
3. E < B < C < D < A
4. A < D < C < E < B
ข้อ 2
สารละลายบัฟเฟอร์ (buffer solution) มีหน้าที่สำคัญที่สุดตามข้อใด?
1. เปลี่ยนค่า pH ของสารละลายให้เป็นกลาง (pH = 7) เสมอ
2. ทำปฏิกิริยากับกรดแก่หรือเบสแก่ เพื่อสร้างเกลือและน้ำ
3. ต้านทานการเปลี่ยนแปลงค่า pH เมื่อมีการเติมกรดหรือเบสลงไปเล็กน้อย
4. เป็นตัวบ่งชี้ (indicator) ที่เปลี่ยนสีตามค่า pH ของสารละลาย
5. ทำให้สารละลายกรดอ่อนแตกตัวได้ 100%
ข้อ 3
สารละลายในข้อใดต่อไปนี้ เมื่อทดสอบด้วยกระดาษลิตมัส จะทำให้กระดาษลิตมัสสีน้ำเงินเปลี่ยนเป็นสีแดง?
1. น้ำสบู่
2. น้ำมะนาว
3. น้ำเกลือ
4. น้ำเปล่าบริสุทธิ์
5. สารละลายเบกกิ้งโซดา
น้องๆ ชาว Dek-D คิดว่าข้อไหนถูกต้อง ถ้ารู้แล้วว่าก็คอมเมนต์ด้านล่างได้เลย!
น้อง ๆ เป็นอย่างไรกันบ้างคะ? กับเรื่องกรด-เบส ในวิชาเคมีวันนี้ “รู้ไว้เผื่อออกสอบ” ครั้งหน้า น้อง ๆ อยากรู้เรื่องไหน มาคอมเมนต์กันด้านล่างได้เลยนะคะ
สำหรับน้องๆ ที่ยังไม่แม่นเนื้อหา ฟิตความพร้อมก่อนสอบด้วย คอร์สพิชิต TCAS เคมี A-Level สรุปเนื้อหาเคมี ม.ปลาย 3 ปี ครบถ้วน ตรงตามหลักสูตรล่าสุด สสวท. ตัวอย่างโจทย์จัดเต็มกว่า 340 ข้อ เทคนิคการทำโจทย์แบบเข้าใจจริง เน้นย้ำจุดที่พลาดได้บ่อยๆ คอร์สนี้สอนโดย อ.เต้ อาจารย์ประจำภาควิชาเคมี จุฬาฯ

ข้อมูลจากhttps://il.mahidol.ac.th/e-media/acid-base/C3jum11.htmhttps://www.scimath.org/lesson-chemistry/item/7071-2017-05-26-15-16-15https://www.scimath.org/lesson-chemistry/item/7887-2018-02-27-03-53-51https://www.chemistryk.comhttps://curadio.chula.ac.th/Images/Class-Onair/ch/2007/ch-2007-12-21.pdfhttps://il.mahidol.ac.th/e-media/acid-base/C12_1.HTMhttps://ngthai.com/science/27553/acid-base/https://www.neonics.biz/buffer/buffer-solution/

0 ความคิดเห็น